Le centre de coordination à Berne compte un ensemble de huit « Clinical Project Managers ». Ces personnes sont chargées du suivi et de la coordination des études cliniques et projets de recherche du SPOG. La cheffe d’équipe, Lara Fux, nous explique ce que font ces spécialistes pour que les études sur le cancer de l’enfant puissent être proposées par le SPOG dans ses neuf hôpitaux membres.
Mme Fux, de combien d’études êtes-vous actuellement responsable avec votre
équipe ?
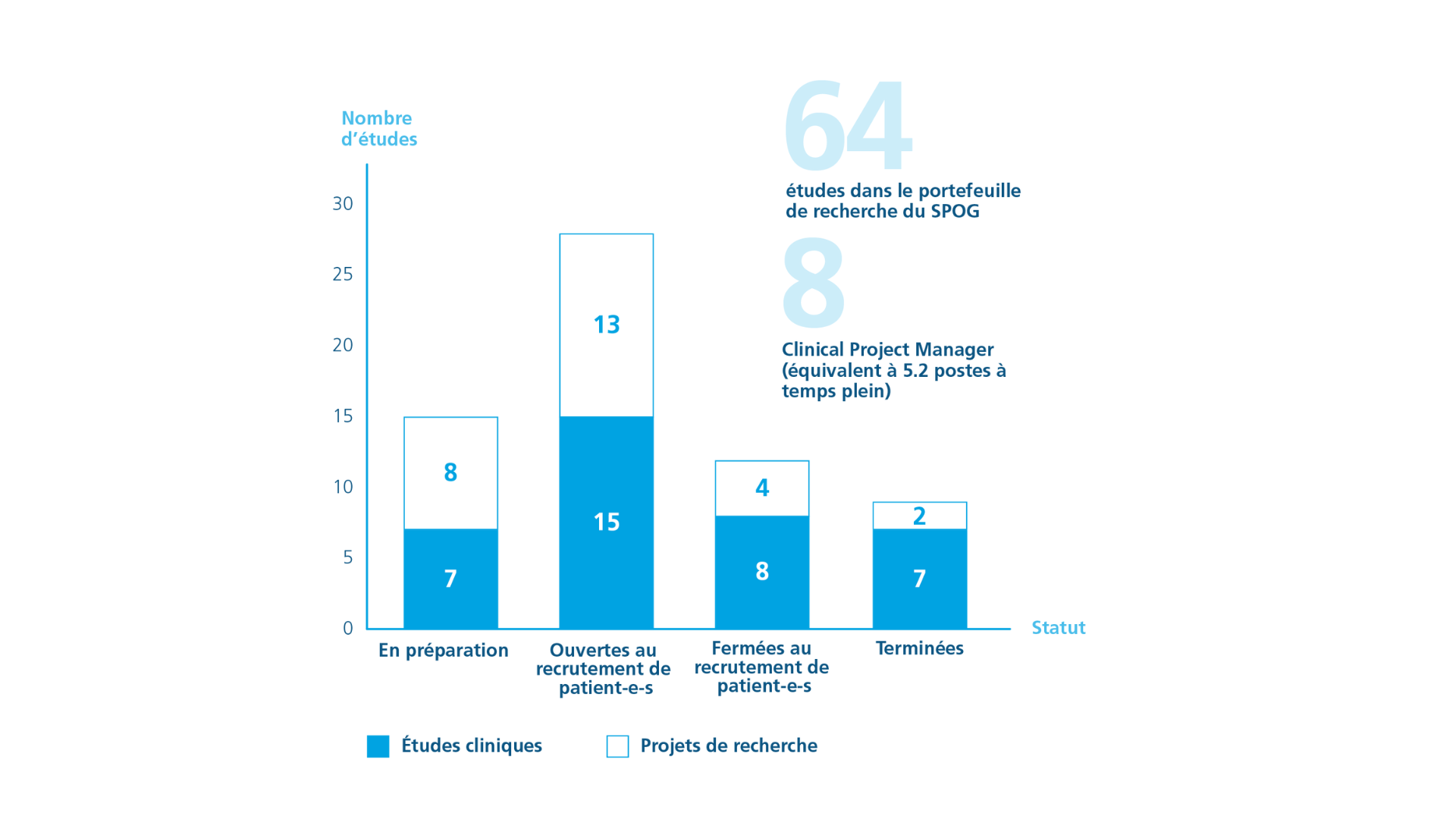
Actuellement, nous assurons le suivi de 64 études, dont la moitié environ est ouverte au recrutement de patient-e-s. Les autres études sont soit en préparation – nous travaillons donc à pouvoir les ouvrir prochainement au recrutement – soit leur phase de recrutement est terminée. Les patient-e-s inclus-es reçoivent déjà leur traitement dans le cadre de ces études et feront ensuite l’objet d’un suivi, après quoi les données seront analysées.
Actuellement, les Clinical Project Managers assurent le suivi de 64 études.
Que fait l’équipe des Clinical Project Managers du SPOG pour les oncologues pédiatriques des hôpitaux membres ?
Les Clinical Project Managers libèrent les équipes de recherche dans les hôpitaux des travaux réglementaires et administratifs de façon à ce que les chercheurs/-euses puissent se concentrer sur le suivi des patient-e-s. Par exemple, nous nous chargeons collectivement pour tous les hôpitaux membres des soumissions et établissements de rapports pour les autorités suisses. Sans notre travail, chaque hôpital devrait le faire soi-même. La coordination des études est centralisée et simplifiée, ce qui améliore l’efficacité et la qualité. Par ailleurs, nous faisons le lien entre les hôpitaux membres et les centres de gestion d’études internationales (promoteurs). En effet, avoir un seul interlocuteur dans chaque pays facilite la tâche des promoteurs internationaux.
« Les Clinical Project Managers libèrent les équipes de recherche dans les hôpitaux des travaux réglementaires et administratifs de façon à ce que les chercheurs/-euses puissent se concentrer sur le suivi des
patient-e-s. »
Pourquoi la plupart des études du SPOG sont-elles des protocoles internationaux ?
Fort heureusement, le cancer est très rare chez les enfants et adolescent-e-s. Pour la recherche, le faible nombre de patient-e-s signifie qu’il est difficile de pouvoir mener des études significatives en Suisse. C’est pourquoi nos protocoles d’études viennent pour la plupart de promoteurs internationaux comme la Grande-Bretagne ou l’Allemagne. Les études sont menées en parallèle dans plusieurs pays, ce qui permet d’augmenter l’effectif de patient-e-s. Grâce à la collaboration internationale, la recherche sur le cancer de l’enfant peut progresser plus rapidement.
Chaque étude du SPOG dispose d’une direction nationale. Comment se passe la collaboration des Clinical Project Managers avec les « National Study Chairs » ?
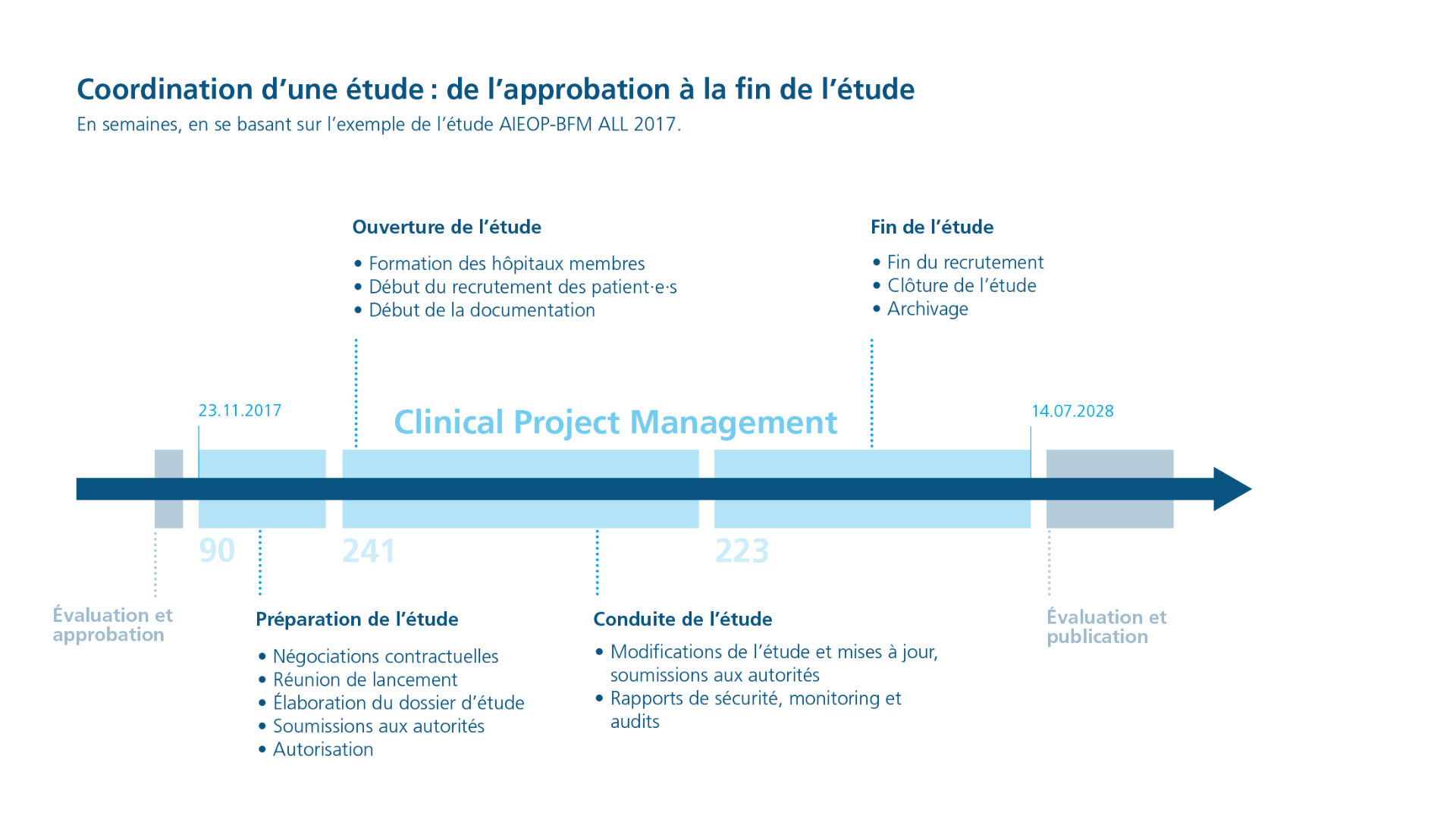
Nous avons une collaboration très étroite, en particulier pendant la phase de préparation à l’ouverture. Nous commençons par une réunion de lancement au cours de laquelle le Clinical Project Manager et la direction de l’étude évoquent et planifient la conduite de l’étude en Suisse. On peut ainsi discuter des médicaments qui sont nécessaires à l’étude ou des analyses qui devront être effectuées pour le diagnostic. Ensuite, la répartition des tâches est simple : la direction de l’étude est responsable de tous les aspects médicaux et le Clinical Project Manager de toutes les questions réglementaires et de la gestion de la qualité.
À quelle fréquence votre équipe est-elle en contact avec les hôpitaux membres ?
Les Clinical Project Managers sont quotidiennement en contact avec les hôpitaux membres. Qu’il s’agisse d’élucider certaines questions ou de déployer le plus rapidement possible de nouvelles découvertes ou des modifications du protocole en Suisse. Pour moi, la collaboration avec les hôpitaux est très constructive et agréable. En définitive, nous avons tous le même objectif – donner un avenir aux enfants et adolescent-e-s atteint-e-s d’un cancer.
« Nous avons tous le même objectif – donner un avenir aux enfants et adolescent-e-s atteint-e-s d’un cancer. »
Pourquoi la préparation d’une étude prend-elle relativement beaucoup de temps ?
Les contrats avec les promoteurs internationaux nécessitent en particulier beaucoup de travail. Sans ces contrats, nous ne pouvons pas soumettre une étude auprès des autorités suisses et par conséquent, nous ne pouvons pas recruter de patient-e-s. Malheureusement, il faut souvent beaucoup de temps pour finaliser ces contrats du fait des législations et directives différentes dans chaque pays.
Comment se passe la collaboration avec Swissmedic et les commissions d’éthique ?
Nous avons établi une bonne collaboration avec Swissmedic et les commissions d’éthique. Grâce à notre expérience de longue date, nous connaissons les exigences de ces autorités et pouvons ainsi préparer en conséquence la documentation relative aux études. En cas de questions sur des cas spécifiques, nous pouvons contacter les différentes autorités pour un échange constructif.
Pourquoi la recherche sur le cancer de l’enfant fait-elle l’objet d’une réglementation si stricte ?
La recherche sur l’être humain est régie par une vaste législation en Suisse. Ce type de recherche est uniquement autorisé s’il est au préalable contrôlé et validé par les autorités. La loi relative à la recherche sur l’être humain en est le pilier fondamental : elle vise à protéger la dignité, la personnalité et la santé des patient-e-s. Les enfants et adolescent-e-s sont considéré-e-s comme des personnes particulièrement vulnérables et la recherche est donc soumise à des directives supplémentaires.
« La recherche sur l’être humain est régie par une vaste législation en Suisse. Ce type de recherche est uniquement autorisé s’il est au préalable contrôlé et validé par les autorités. »
Le travail au centre de coordination est-il également contrôlé ?
Le SPOG organise des audits réguliers, tant au centre de coordination que dans les hôpitaux membres. Ces audits sont réalisés par des prestataires de services externes et indépendants. Les résultats permettent au SPOG de maintenir la qualité de la conduite des études et de l’améliorer en continu.
Par ailleurs, les autorités suisses et les sponsors internationaux sont autorisés à inspecter à tout moment le centre de coordination du SPOG et les hôpitaux membres. Swissmedic procède régulièrement à de telles inspections.
Quelles modifications ont été apportées à la coordination d’études ces dernières années ?
La recherche clinique est – à juste titre – un domaine fortement réglementé. Au cours des dernières années, les lois nationales et internationales, ainsi que leur application, sont devenues de plus en plus strictes. Il est rare qu’une exigence soit abandonnée lors de la révision des lois ou des directives. Il devient donc de plus en plus complexe de mener des études et le fardeau administratif s’en trouve accru, tant pour les hôpitaux que pour le centre de coordination.
Que reste-t-il à faire pour les Clinical Project Managers une fois qu’une étude est ouverte ?
Nous assurons le suivi des études à travers tous les cycles de leur réalisation. Après l’ouverture, la structure d’une étude peut être modifiée, un nouveau bras peut être ouvert ou l’étude peut être prolongée. Nous soumettons au préalable aux autorités suisses toutes ces modifications essentielles à des fins d’approbation. De plus, nous informons les autorités en continu sur tous les aspects de sécurité des études cliniques. À cet égard, nous présentons un rapport au moins une fois par an.
Quelle est la durée réelle d’une étude ?
La durée d’une étude peut varier considérablement en fonction de son objectif. Les études cliniques qui testent et comparent différents traitements ont en général une phase de recrutement d’environ cinq ans, puis une phase de suivi des patient-e-s d’environ trois ans.
Il est toutefois également important d’évaluer les éventuels effets à long terme d’un cancer et de ses traitements. Les projets avec un tel objectif peuvent avoir une durée illimitée.
Les Clinical Project Managers assurent le suivi des études à travers tous les cycles de leur réalisation.
Que se passe-t-il lorsqu’une étude arrive à son terme ?
La clôture d’une étude comprend plusieurs étapes. Tout d’abord, le recrutement est arrêté, ce qui signifie qu’aucun-e patient-e supplémentaire n’est inclus-e dans l’étude. Les patient-e-s déjà inclus-es finissent leur traitement et sont suivi-e-s pendant plusieurs années afin d’évaluer comment ils/elles se portent. Une fois ce suivi terminé, l’étude est officiellement terminée. Toutes les données disponibles sont alors analysées et les résultats sont publiés. L’étude est ainsi définitivement clôturée.
Comment les résultats des études sont-ils diffusés ?
Pour les études cliniques, un rapport final doit être rédigé dans un délai d’un an après la fin de l’étude et présenter toutes les découvertes de l’étude. Ce rapport est mis à la disposition des médecins des hôpitaux cliniques et doit être soumis aux autorités suisses, qui en prennent connaissance. Par ailleurs, les résultats des études sont habituellement publiés dans des revues scientifiques accessibles à tous les oncologues. Désormais, on dispose également de résumés des résultats des études cliniques dans un langage compréhensible par tous. Ces résumés sont publiés sur la plateforme dédiée à la recherche sur l’être humain en Suisse.
Quels sont les difficultés du travail de Clinical Project Manager ? Et quels sont les aspects positifs ?
Ce qu’il y a de formidable dans le Clinical Project Management, c’est que notre travail permet aux enfants et adolescent-e-s atteint-e-s d’un cancer d’avoir accès au meilleur traitement possible, basé sur les dernières avancées scientifiques. Cette pensée nous motive au quotidien et nous aide à être productifs. Ce qui est frustrant, c’est quand la participation à une étude n’est pas possible car l’ouverture est retardée du fait des négociations de contrats.
« Ce qu’il y a de formidable dans le Clinical Project Management, c’est que notre travail permet aux enfants et adolescent-e-s atteint-e-s d’un cancer d’avoir accès au meilleur traitement possible, basé sur les dernières avancées scientifiques. »
Lara Fux
Lara Fux, cheffe d’équipe du Clinical Project Management au centre de coordination du SPOG
Clinical Project Manager
Les Clinical Project Managers du centre de coordination du SPOG assurent le suivi et la coordination des études cliniques et projets de recherche, notamment sur le plan réglementaire. Ils s’occupent de la coordination complexe et continue avec les partenaires internationaux et assument une grande responsabilité en matière de conformité légale de la conduite des études en Suisse. Les Clinical Project Managers ont besoin de connaissances de base en sciences naturelles et sciences de la santé afin de comprendre les documents relatifs aux études et les procédures de la recherche clinique.
Brigitte Casanova
Brigitte Casanova accompagne les projets de communication du SPOG, en tant que germaniste, elle complète l'équipe axée sur les sciences naturelles du centre de coordination.
Autres articles de Brigitte Casanova